Hành trình của vắc xin Covid-19 Nanocovax, lấy hiệu quả, an toàn làm tiêu chuẩn hàng đầu
Trong thử nghiệm giai đoạn 3 trên 13.000 tình nguyện viên, vắc xin Nanocovax được kỳ vọng có khả năng bảo vệ cao tương đương các vắc xin trên thế giới.
Công nghệ protein tái tổ hợp ít tác dụng phụ
Việt Nam đang có bước tiến khá nhanh trong sản xuất vắc xin, ở đó vắc xin Nanocovax của Công ty CP công nghệ sinh học dược Nanogen hiện chiếm giữ lợi thế lớn khi đang đi đến giai đoạn cuối cùng của thử nghiệm lâm sàng giai đoạn 3.
TS Hồ Nhân, Tổng Giám đốc Nanogen cho biết, vào thời điểm tháng 4/2020, việc lựa chọn công nghệ sản xuất vắc xin trong giai đoạn đầu gần như "ném đá dò đường". Tuy nhiên Nanogen chỉ mất 1 tuần để lên ý tưởng thiết kế.

Ông Hồ Nhân (CEO Nanogen) trao đổi với Thủ tướng Phạm Minh Chính trong chuyến thăm ngày 26/6/2021
Với thế mạnh gần 20 năm chuyên sản xuất nguyên liệu dược và các thuốc đặc trị viêm gan B, C, thiếu máu, ung thư… bằng công nghệ DNA/protein tái tổ hợp, Nanogen quyết định chế tạo vắc xin Covid-19 từ công nghệ mình đã làm chủ.
Các nhà khoa học của Nanogen dùng đoạn gene của virus mã hóa, tạo ra protein gai S giống hệt gai trên SARS-CoV-2, sau đó thu hoạch, tinh sạch, trộn cùng tá dược để tạo nên vắc xin thành phẩm.
Do không dùng bất kì thành phần sống nào của virus nên trong các giai đoạn thử nghiệm, vắc xin Nanocovax được đánh giá an toàn và không gây ra bất kì tác dụng phụ nghiêm trọng nào.
"Mục tiêu mà Nanogen hướng tới là tạo nên vắc xin an toàn, có thể bảo vệ cơ thể 100%", ông Hồ Nhân chia sẻ.
Nanocovax được nghiên cứu kỹ lưỡng và thử nghiệm đúng theo các quy chuẩn quốc tế. Trong giai đoạn thử nghiệm tiền lâm sàng, vắc xin được thử nghiệm trên khỉ đuôi lợn, chuột nhắt, chuột cống, chuột lang và thỏ.
Từ ngày 17/12/2020 - 7/2/2021, Học viện Quân y tiêm thử nghiệm lâm sàng giai đoạn 1 vắc xin Nanocovax trên 60 tình nguyện viên với 3 nhóm liều 25mcg, 50mcg và 75mcg để đánh giá tính an toàn.
Kết quả, vắc xin có độ an toàn đạt 100%, hiệu quả bảo vệ người tiêm không bị nhiễm virus SARS-CoV-2 lên đến 90% và tất cả đều sinh miễn dịch tốt.
Đến ngày 26/2/2021, Nanocovax bắt đầu thử nghiệm lâm sàng giai đoạn 2 với 554 tình nguyện viên tham gia. Kết quả, vắc xin an toàn, 100% tình nguyện viên đều sinh miễn dịch. Đặc biệt tỉ lệ chuyển đổi huyết thanh của Nanocovax đạt đến 99,4% và kháng thể sinh ra có thể chống lại chủng Vũ Hán, Anh, Nam Phi.
Các phản ứng phụ của Nanocovax thậm chí còn thấp hơn nhiều loại vắc xin hàng đầu thế giới đang được sử dụng hiện nay và chưa ghi nhận trường hợp nào sốc phản vệ.
Kết quả cho thấy, ở ngày thứ 35, liều 75mcg sinh miễn dịch cao nhất (53), liều 25mcg và 50mcg tương đương nhau (lần lượt 29 và 36). Tuy nhiên đến ngày thứ 42, liều 25mcg lại sinh miễn dịch tốt nhất (105), liều 50cmg (79) và 75mcg (92). Do đó Hội đồng Đạo đức, Bộ Y tế quyết định chọn duy nhất nhóm liều 25mcg cho nghiên cứu giai đoạn 3.
Đảm bảo an toàn, chính xác cao
Ngày 11/6, Bộ Y tế chính thức phê duyệt đề cương thử nghiệm giai đoạn 3 vắc xin Nanocovax trên quy mô 13.000 người, trong đó giai đoạn 3a tiêm 1.000 người, giai đoạn 3b tiêm 12.000 còn lại. Đây là giai đoạn quan trọng nhất để đánh giá hiệu quả, độ an toàn của vắc xin.
Ban đầu, Bộ Y tế dự định triển khai thử nghiệm pha 3a, khi có kết quả sẽ đánh giá trước khi tiêm giai đoạn 3b. Tuy nhiên sau khi có ý kiến chỉ đạo của Thủ tướng, ngày 25/6, Hội đồng Đạo đức đã đồng ý đẩy nhanh tiến độ thử nghiệm, tiêm luôn vắc xin cho 12.000 tình nguyện viên còn lại. Bộ Y tế cho biết, dù đẩy nhanh nhưng không bỏ sót giai đoạn, ưu tiên cao nhất việc đảm bảo an toàn và chính xác trong nghiên cứu.
Hiện tại, 1.000 tình nguyện viên ở giai đoạn 3a đã tiêm xong mũi 2, các tình nguyện viên giai đoạn 3b dự kiến tiêm xong mũi 1 trước ngày 15/7 và hoàn tất mũi 2 trước ngày 15/8 (trong đó Hà Nội 2.000 tình nguyện viên, Hưng Yên 4.000, Long An 2.000 và An Giang 4.000).
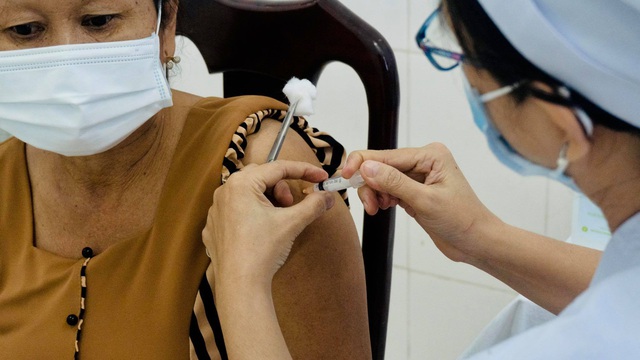
Người dân tiêm thử nghiệm lâm sàng pha 3, tại Bến Lức, Long An
Dự kiến trong giai đoạn 3, vắc xin Nanocovax có thể đạt hiệu quả bảo vệ khoảng 90%, tương đương với các vắc xin trên thế giới. Hiệu quả trước biến thể Delta cũng được thử nghiệm trong giai đoạn 3.
Đến khoảng tháng 9, nhóm nghiên cứu sẽ có dữ liệu báo cáo về kết quả ban đầu thử nghiệm giai đoạn 3.
Phía Nanogen cho biết, nếu kết quả pha 3 tốt, công ty sẽ tiếp tục kiểm định kết quả với các cơ quan độc lập, sau đó mới bắt đầu quy trình xin Bộ Y tế và Hội đồng Đạo đức cấp phép khẩn có điều kiện cho phép lưu hành Nanocovax.
Trong thử nghiệm giai đoạn 3, sẽ có thêm chuyên gia của Tổ chức Y tế Thế giới cùng đồng hành để hỗ trợ, đánh giá chất lượng vắc xin Nanocovax.
Hiện tại, Nanogen có 4 nhà máy, công suất từ nay đến cuối năm có thể đạt 50 - 100 triệu liều vắc xin phục vụ nhu cầu trong nước.

Đội ngũ nghiên cứu Nanogen hoạt động ngày đêm trước tình hình dịch bệnh căng thẳng